2021年人教版化学九年级下册 9.3.2溶液的浓度
一、选择题
1.下列图象能正确反映其对应操作中各量变化关系的是( )
A.向pH=3的稀盐酸中不断加水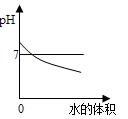
B.向接近饱和的硝酸钾溶液中不断加入硝酸钾固体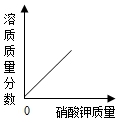
C.高温煅烧一定质量的石灰石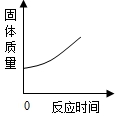
D.在部分变质的NaOH溶液中加稀盐酸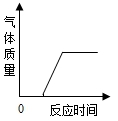
3.现有一定质量的KOH和K₂CO₃混合物,测得其中钾元素质量分数为60%,将其放入90g稀HCl中恰好完全反应,得到100g不饱和溶液和3g气体,则所得溶液中溶质的质量分数是( )
A. 7.8%
B. 13.8%
C. 17.4%
D. 14.9%
4.下列是小明“配制50g溶质质量分数为20%的氯化钠溶液”的实验过程。正确的是( )
A. 计算需要氯化钠10g、水40g
B. 将氯化钠放到托盘天平右盘称量
C. 将氯化钠放在量筒中溶解
D. 将配制好的溶液转移一半后,小明认为剩余溶液溶质质量分数为10%
5.下列图示与对应的叙述相符的是( )
A. 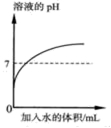 常温下向稀盐酸中不断加水
常温下向稀盐酸中不断加水
B. 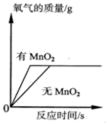 用两份等质量、等溶质的质量分数的双氧水制取氧气
用两份等质量、等溶质的质量分数的双氧水制取氧气
C. 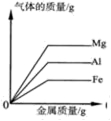 向等质量、等溶质的质量分数的三份稀盐酸中分别加入不同的金属
向等质量、等溶质的质量分数的三份稀盐酸中分别加入不同的金属
D. 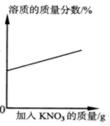 20℃时,向一定量的接近饱和的硝酸钾溶液中加入硝酸钾固体
20℃时,向一定量的接近饱和的硝酸钾溶液中加入硝酸钾固体
二、填空题
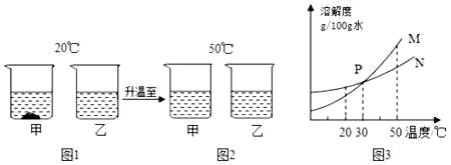
1.下表为两种物质在不同温度时的溶解度。
|
温度/℃ |
|
20 |
40 |
60 |
80 |
100 |
|
溶解度/g |
KCl |
34.0 |
40.0 |
45.6 |
51.5 |
56.7 |
|
KNO₃ |
31.6 |
63.9 |
110 |
169 |
246 |
(1)60℃时,KCl的溶解度是g;
(2)40℃时,将30g KCl加入到50g水中,充分溶解后所得溶液是溶液(填写“饱和”或“不饱和”);
(3)将20℃时KNO₃和KCl的两种饱和溶液升温至60℃,则两种溶液的溶质质量分数大小关系是:KNO₃KCl(填写“>”、“<”或“=”)。
2.配制50g质量分数为10%的氢氧化钠溶液,下列失误会导致所配溶液溶质质量分数偏大的是。
A.装瓶时,有溶液洒出 B.将量筒中的水倒入烧杯时有水溅出 C.溶解时未用玻璃棒搅拌 D.。
3.A、B、C、D、E、F、G为常见的物质,其中B、E、G属于单质,反应②是炼铁工业中的主要反应,如图是它们之间的相互转化关系。请回答:
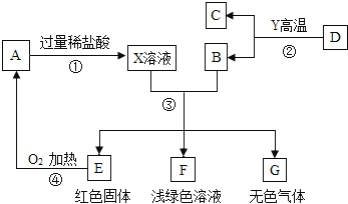
(1)写出物质的化学式:A:B:。
(2)写出反应①的化学方程式,
(3)C物质固态时的名称,该固体物质在实际生活中的一种用途是。
(4)上图转化中产生无色气体G的原因是。
4.水是人及一切生物生存所必需的,为了人类和社会经济的可持续发展,我们应该了解一些有关水的知识。请你回答:
(1)天然水中含有许多杂质,可利用吸附、沉淀、过滤和蒸馏等方法净化,其中净化水程度最高的方法是;除去水中难溶性固体杂质的操作是, 此操作中要用到玻璃棒,其作用是。
(2)生活中可以采用区分硬水和软水,可以通过加入来吸附水中有异味的物质。
(3)如图是电解水实验装置。下列关于电解水实验的叙述中,正确的是(填序号)。
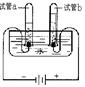
A.该实验可证明水由氢元素和氧元素组成
B.试管a中收集的气体是氧气
C.试管a和试管b中收集的两种气体的质量比是2:1
D.在水中加少量稀硫酸可增强水的导电性
(4)用氯化钠固体加水溶解,配制50g质量分数为6%的氯化钠溶液的过程中,若量取水时俯视读数,其他操作正确,则配制的氯化钠溶液中溶质质量分数(选填“变大”、“变小”或“不变”)。若用上述配好的6%的氯化钠溶液(密度为1.04g/cm³)来配制50g质量分数为3%的氯化钠溶液,需要其体积为(计算结果精确到0.1)。
三、按要求做题
1.配制100g溶质质量分数为20%的稀硫酸,需98%的浓硫酸(密度为1.84g/cm³)的体积和水的质量分别是多少?(计算结果保留一位小数)
2.有碳酸镁与氧化镁的混合物共重12.4克,把该混合物加入到192克稀盐酸中恰好完全反应,称得反应后溶液的质量为200克。试计算反应后所得溶液中溶质的质量分数。(写出具体计算过程)