课程内容
《脂肪烃(二)》
三、炔烃
概念:分子里含有碳碳三键的一类脂肪烃称为炔烃。
炔烃的通式:CnH2n-2(n≥2)
炔烃的通性:
(1)物理性质:随着碳原子数的增多,沸点逐渐升高,液态时的密度逐渐增加。
C小于等于4时为气态
(2)化学性质:能发生氧化反应,加成反应。
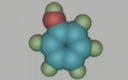
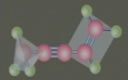
1、乙炔的结构
2、乙炔的实验室制法:
A、原料:
碳化钙(CaC2)与H2O
B、反应原理:
CaC2+2H-OH→C2H2↑+Ca(OH)2
C、装置:
广口瓶(锥形瓶或圆底烧瓶)+分液漏斗
D、收集方法:采用排水集气法收集
实验说明:
(1)反应装置不能用启普发生器,改用广口瓶和分液漏斗,因为:
a、碳化钙与水反应较剧烈,难以控制反应速率;
b、反应会放出大量热,如操作不当,会使启普发生器炸裂。
(2)实验中常用饱和食盐水代替水。
目的:降低水的含量,得到平稳的乙炔气流。
(3)制取时在导气管口附近塞入少量棉花。
目的:为防止产生的泡沫涌入导管。
(4)纯净的乙炔气体是无色无味的气体。用电石和水反应制取的乙炔,常闻到有恶臭气味,是因为在电石中含有少量硫化钙、砷化钙、磷化钙等杂质,跟水作用时生成H2S、A5H3、PH3等气体有特殊的气味所致。
3、物理性质:乙炔是无色、无味的气体,微溶于水。
4、乙炔的化学性质:
(1)氧化反应:
可燃性:在氧气中燃烧生产二氧化碳和水。
火焰明亮,并伴有浓烟。
乙炔能使酸性KMnO4溶液褪色。
(2)加成反应
a、使溴水褪色
b、催化加氢
c、与HX等的反应
四、脂肪烃的来源及应用:
1、来源:石油、天然气、煤等
常、减压分馏;催化裂化(裂解)、催化重整;煤的干馏、液化等。
2、应用:气态烯烃是最基本的化工原料
石油通过常压分馏可以得到石油气、汽油、煤油、柴油等;而减压分馏可以得到润滑油、石蜡等分子量较大的烷烃;通过石油的催化裂化及裂解可以得到较多的轻质油和气态烯烃,气态烯烃是最基本的化工原料;而催化重整是获得芳香烃的主要途径。
天然气是高效清洁燃料,主要是烃类气体,以甲烷为主。
煤也是获得有机化合物的源泉。通过煤焦油的分馏可以获得各种芳香烃;通过煤矿直接或间接液化,可以获得燃料油及多种化工原料。