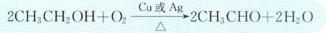课程内容
《生活中两种常见有机物-乙醇》
一、物理性质
颜色:无色透明
气味:特殊香味
状态:液体
挥发性:易挥发
密度:比水小
溶解性:跟水以任意比互溶,能够溶解多种无机物和有机物
走进生活:
Q1:如何检验酒精是否含水?
用无色硫酸铜检验水分子存在现象:白色变蓝色
Q2:如何由普通酒精制取无色酒精?
用普通酒精与新制石灰混合蒸馏,可得无水酒精。
分子结构
分子式:C2H6O
结构式: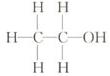
结构简式:CH3CH2OH或C2H5OH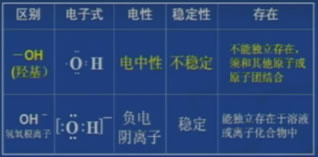
实验:
乙醇与金属钠的反应
金属钠的变化:沉入底部,不熔成小球,不发出响声
气体燃烧现象:燃烧时发出淡蓝色火焰
检验产物:干燥小烧杯有水珠,澄清石灰水无明显变化,说明生成的气体是氢气。
想一想:实验现象说明了什么问题?
1、钠浮在水面上,而沉在乙醇中说明:水的密度>钠的密度>乙醇的密度
2、钠与乙醇的反应速率比钠与水的反应速率慢,说明羟基上的H原子与水中H原子的活泼性:乙醇<水
3、乙醇的性质是由它的结构决定的
观察比较:乙醇和乙烷
烃分子中的H原子被其他或原子团所取代而生成一系列化合物,称为烃的衍生物。
决定有机化合物化学性质的原子或原子团称为官能团。
乙醇的氧化反应
a、燃烧反应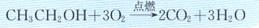
现象:发出淡蓝色火焰,并放出大量热
b、催化氧化
现象:光亮的铜丝加热由红变黑,迅速插入到乙醇中,变回红亮,同时闻到刺激性气味。
结论:乙醇被催化剂氧化成乙醇
反应方程式: