课程内容:
《性质活泼的氧气(2)》
一、实验探究
【实验2-5】
(1)在试管中加入5ml 5%的过氧化氢溶液,把带火星的木条伸入试管,木条是否复燃?
(2)向上述试管中加入少量二氧化锰,把带火星的木条伸入试管。观察发生的现象。
探究可知: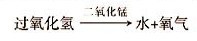
思考:二氧化锰在反应中担任什么角色?起什么作用?
二、催化剂
1.定义:在化学反应中能改变其它物质的化学反应速率,而本身的质量和化学性质在化学反应前后都没有变化的物质叫催化剂。
2.注意:
(1)催化剂参加了化学反应;
(2)反应前后,催化剂的质量和化学性质不变;
(3)催化剂通过改变反应的途径而改变(加快或减慢)反应的速率;
(4)催化剂不能决定化学反应能否发生,且不能改变产物的质量。
三、氧气的实验室制法反应原理
过氧化氢→(二氧化锰)水+氧气
高锰酸钾→(加热)酸锰钾+二氧化锰+氧气
氯酸钾→(二氧化锰+加热)氯化钾+氧气
四、分解反应
由一种反应物生成两种或两种以上其他物质的反应叫分解反应。
思考并讨论下列问题:
1.你打算用什么药品来制取氧气?你认为需要哪些仪器才能制取氧气?
2.一套制气装置,你认为应该包含哪些装置?怎样来组装你所需要的仪器,组装时需要注意什么?
3.你认为制取气体前,需不需要检查装置的气密性?如果需要,该怎么去检查呢?
4.气体常见的收集方法有哪些?
5.你认为用什么方法去收集所制得的氧气?你认为什么时候收集氧气最合适?(排水法收集时)
6.怎样才知道集气瓶中已经装满了氧气?
7.实验结束时应该怎样去操作?(排水法收集时)
制氧气的药品:
过氧化氢、二氧化锰、高锰酸钾、氯酸钾
制氧气所需要仪器:
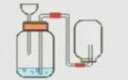
(1)过氧化氢溶液和二氧化锰:
试管、铁架台(带铁夹)、带导气管的橡皮塞(双孔)、集气瓶、水槽、药匙
(2)高锰酸钾固体或氯酸钾和二氧化锰
试管、铁架台(带铁夹)、酒精灯、带导气管的橡皮塞(单孔)、集气瓶、水槽、药匙
【实验装置】
制取气体的装置一般包含发生装置和收集装置两部分。
发生装置→收集装置
组装仪器一般是按从左到右,从上到下的顺序进行的。
气体常见的收集方法:
1.排水法——适于气体不易或难溶于水且不与水反应
2.排空气法:
(1)向上排空气法——适于气体的密度比空气大且不与空气反应
(2)向下排空气法——适于气体的密度比空气小且不与空气反应
3.氧气的手机方法:可用排水法或向上排空气法收集氧气
检验及验满(排气法):
检验:将带火星的木条伸入集气瓶中,若木条复燃,则收集的气体是氧气。
验满:将带火星的木条放在(或靠近)集气瓶口,若木条复燃,则已收集满氧气。
【注意】实验完毕,先撤导管,后移酒精灯。收集满的氧气,应放在桌面上,并用毛玻璃片盖上。
原因:防止试管冷却后,水槽内的水沿导管上升,进入导管,使试管炸裂
制取氧气的操作步骤(加热高锰酸钾):
检查气密性→装药品→固定装置→加热(要预热)→收集氧气→移出导管(排水法收集时)→熄灭酒精灯
加热固体方法制取氧气装置的注意事项:
1.酒精灯中酒精量不能超过其容积的2/3;
2.药品尽量平铺在试管的底部;
3.用酒精灯外焰对准盛药品部位加热;
4.铁夹夹在离管口约1/3处(或试管中上部);
5.试管管口略向下倾斜;
6.伸入试管中的导管稍露出橡皮塞;
7.排水法收集氧气实验结束时,应先从水槽中移出导气管,再熄灭酒精灯。
8.当用高锰酸钾制取时,应在试管中管口附近塞一团棉花。
氧气的工业制法:
1.分离液态空气法——根据液态氢与液态氧的沸点不同
2.利用分离技术膜
在一定压力下,让空气通过具有富集氧气功能的薄膜,可得到含氧量较高的富氧空气。
此内容正在抓紧时间编辑中,请耐心等待
赵老师
男,中教中级职称
在学生感兴趣的基础上授之以渔。教无定法,因材施教,让学生找到适合自己的学习方法。